HDAC是表观遗传调节剂,不仅调节染色质中组蛋白的乙酰化水平,还调节多种与肿瘤进展、细胞周期控制、细胞凋亡、血管生成以及细胞侵袭等相关的蛋白质。由于HADC在基因表达中的基本作用以及对组蛋白和非组蛋白的不同影响, HDAC已成为治疗多种恶性肿瘤的理想靶点,HDAC抑制剂被认为是最有前景的抗癌药物之一。
HDAC作用机理
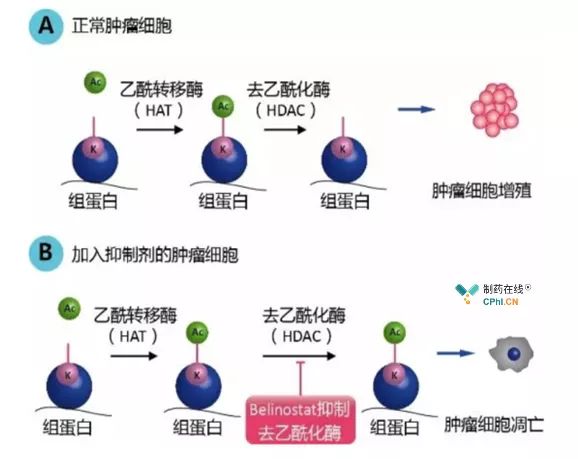
图1 HDAC抑制剂作用机制
HDAC (Histone Deacetylase),全称组蛋白去乙酰化酶,是组蛋白修饰过程中一类重要的酶。HDAC可以去除组蛋白赖氨酸(Lysine)残基上的乙酰基,改变电荷使染色体结构更加紧密,从而抑制基因的转录表达。
根据酵母蛋白的同源性,可将目前在人体中已发现的18种HDAC分为四类(Class I、II、III 和 IV)。其中,I类(HDAC1,2,3,8)为专门表达于细胞核的HDAC,II类(HDAC4,5,6,7,9和10) 可以在细胞核与细胞质间移动,IV类(HDAC11)与I类和第II类相似,但拥有更高的组织特异性。III类(SIRT1,2,3,4,5,6和7)Sirtuins是NAD+依赖型蛋白,非金属依赖型,也没有锌离子催化位点。对应地,主流的HDAC抑制剂也有四大种类。
目前主流的HDAC抑制剂针对第一二四类,按照与Zn2+结合的官能团的化学结构,主要包括羟肟酸类、环四肽类、短链脂肪酸和苯酰胺类。其中前三大类化合物抑制第一类和第二类所有HDAC亚型,属于HDAC非选择性抑制剂。苯酰胺类主要抑制第一类HDAC中HDAC1、HDAC2、HDAC3和部分第二类HDAC,具有选择型,可靶向作用于目标位点。胃癌、直肠癌中HDAC家族表达明显高于正常水平。目前,HDACi在外周T细胞淋巴瘤(PTCL)治疗领域取得了显著进展。FDA已经批准HDACi贝利司他、伏立诺他与罗米地辛用于治疗复发/难治性PTCL(rr-PTCL)。而HDACi和化疗联用后,其疗效较为突出。NMPA已经批准西达本胺用于治疗复发/难治性PTCL。因此,许多药物开发者认为HDAC抑制剂在癌症治疗方面具有巨大研发价值。
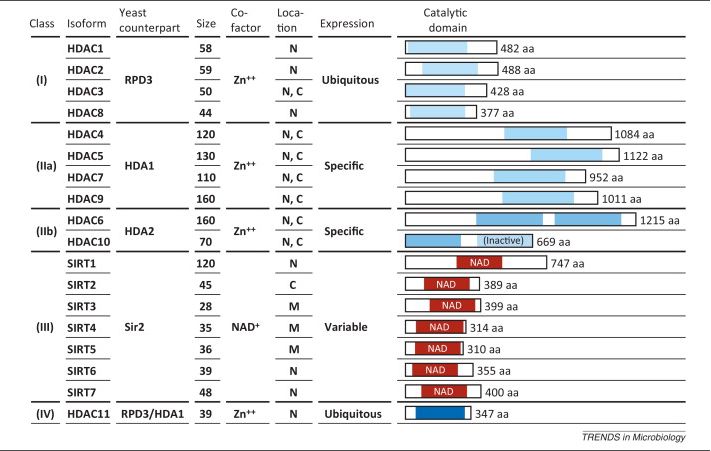
来源:Reactivation oflatent HIV by histone deacetylase inhibitors.
HDAC抑制剂研究进展
作为一个成熟的抗癌靶点,HDAC抑制剂目前的适应症主要集中在血液疾病,且大部分产品都在进行新的适应症的临床试验,如乳腺癌,非小细胞肺癌,胰腺癌等。随着研究深入,其适应症范围可能增加。
目前,全球已经批准上市的HDAC抑制剂共有5款。伏立诺他、罗米地辛、贝利司他、帕比司他为美国FDA批准上市,用于临床治疗外周T细胞淋巴瘤、皮肤T细胞淋巴瘤和多发性骨髓瘤;西达本胺(商品名:爱普莎)由我国NMPA批准上市,用于外周T细胞淋巴瘤和乳腺癌。其中,除西达本胺为HDAC I类及HDAC10亚型选择性抑制剂外,其它四个均为HDAC泛抑制剂。它们在抑制HDAC I类和 IIb类的同时,对HDAC Ⅱa或HDAC IV类,如HDAC5、HDAC9、HDAC11亚型等也有抑制活性,且对HDAC Ⅱa和Ⅳ类酶的抑制存在更多潜在毒副作用。
目前全球处于临床阶段的HDAC抑制剂共有44项,进入2/3期的药物情况如表2所示。在未上市的药物之中,由Italfarmaco公司开发的泛HDAC抑制剂Givinostat,其针对适应症慢性骨髓增值性肿瘤已进入II期临床试验;其针对杜氏肌营养不良症(DMD)正在开展关键III期临床试验,预计进行到2022年3月。由MEI制药开发、后由Helsinn获得其全球研发和商业化权利的口服HDAC抑制剂Pracinostat, 其联合阿扎胞苷治疗成人急性髓细胞白血病的III期临床试验由于缺乏疗效被IDMC建议提前终止。

表2 进入2/3期临床试验的HDAC抑制剂(截止2020年)
去除同一药物申请的不同适应症、以及停止临床实验的药品之后,国内适应症为血液肿瘤相关疾病的药物处于临床阶段的主要有8个。如表3所示,进展最快的恩替诺特和艾贝斯他均已进入临床III期;双替尼他正在开展临床II期。
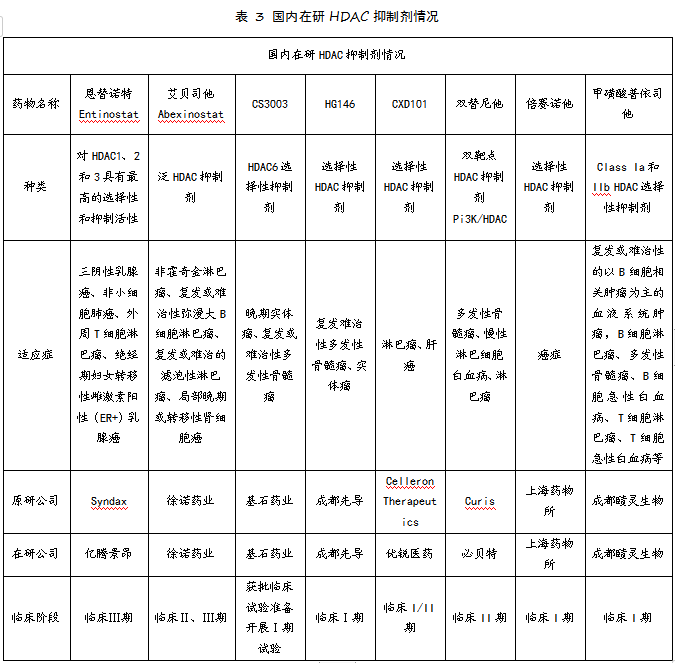
表3 国内在研HDAC抑制剂情况
在处于临床阶段的药物中, 恩替诺特(Entinostat)选择性较高,对HDAC1、2和3具有最高的选择性和抑制活性。亿腾景昂从美国合作方Syndax引进该项目的授权,目前布局乳腺癌和胃癌两大治疗领域的产品, 正在进行联合内分泌治疗激素受体阳性晚期乳腺癌患者的随机III期临床试验,已完成入组375人。自2004年至今,Entinostat在Clinical Trials 登记的临床试验达到了45项,涵盖实体瘤和血液瘤领域。Entinostat针对晚期HR+乳腺癌的II期试验显示依西美坦联合恩替诺特可显著改善无进展生存期(progression-freesurvival,PFS)和总生存期(overall survival,OS),然而根据2021年2月SABCS大会发布的进展,其III期试验数据显示实验组与安慰剂组PFS分别3.3月和3.1月,OS分别为23.4月和21.7月,差别无统计学意义。
艾贝司他(Abexinostat)由徐诺药业联合创始人吴文涛于2017年从美国艾伯维获得这款抗肿瘤新药的全球权益,是一种口服有效的强效泛HDAC抑制剂。目前,艾贝司他在美国、中国、欧洲等地同时开展临床试验,主要适应症包括肾癌、淋巴瘤、肉瘤、血液肿瘤、甲状腺癌、乳腺癌、卵巢癌等。其中,艾贝司他单药治疗复发/难治性弥漫大B细胞淋巴瘤,艾贝司他片治疗复发或难治性滤泡性淋巴瘤正在进行II期临床试验,艾贝司他与帕唑帕尼联用治疗局部晚期或转移性肾细胞癌已进入III期试验。
双替尼他为广州必贝特医药开发的HDAC/PI3K双靶点抗癌一类新药,通过破坏肿瘤细胞信使网络抑制淋巴瘤和骨髓瘤的生长,或导致肿瘤消退。其Ⅰ期临床初步结果显示治疗非霍奇金淋巴瘤安全有效。注射用双替尼他治疗复发或难治性外周T细胞淋巴瘤;治疗复发或难治性滤泡性淋巴瘤、慢性淋巴细胞白血病/小淋巴细胞淋巴瘤、淋巴浆细胞样淋巴瘤/华氏巨球蛋白血症和边缘区淋巴瘤等适应症,均于2021年进入临床II期试验阶段。注射用双替尼他治疗复发或难治弥漫大B细胞淋巴瘤正在开展临床II期试验,2020年6月第一例受试者入组。
未来发展方向
随着5个成功上市的HDAC药物在多种亚型血液肿瘤的临床治疗取得突破, T 细胞淋巴瘤和多发性骨髓瘤患者的预后获得了极大的改善,HDAC生物学领域已经取得了许多初步性成功。然而由于赖氨酸翻译后修饰、表观遗传转录调控和非表观遗传细胞信号级联反应的复杂性,许多挑战仍然存在。研究结果也显示HDAC抑制剂治疗非血液实体肿瘤效果不佳,至今仅有西达本胺获批应用于乳腺癌适应症。且目前可用的HDAC抑制剂大多是非异构体选择性的,存在对实体瘤效果不佳、疗效有限、耐药性和毒性及严重不良反应等缺点。
为了在提高活性增强疗效的同时避免其他靶点带来的毒性,开发具有良好活性和高选择性的HDAC抑制剂成为了目前重要的研发方向。例如赜灵生物的在研药物甲磺酸普依司他,为高选择性ClassI 和Class II b HDAC抑制剂,其临床批件申请适应症为复发或难治性的以B细胞相关肿瘤为主的血液系统肿瘤。目前已启动I期临床,计划在以难治亚型取得上市后快速拓展适应症。但由于HDAC的亚型较多,且HDAC在体内多以复合物形式存在,开发高亚型选择性的HDAC抑制剂在实际研究中仍然面临很大的挑战。
开发双(多)靶点抑制剂也是HDAC抑制剂的另一研发方向。若这两(多)个靶点具有协调效应,可以预测将会发挥更好的药效。例如:如Curis公司的CUDC-101(HDAC\EGFR\HER2)和CUDC-907(HDAC\PI3K)(国内权益被广州必贝特医药引进),德国4SC的4SC-202(HDAC\LSD1)以及Imbrium公司的Tinostamustine(HDAC\DNA)等已经完成临床I期研究,部分已进入临床II期。
此外,联合用药是目前HDAC抑制剂在实体瘤等其他适应症拓展上的重要途径,包括与内分泌治疗、放化疗、蛋白酶、激酶等抑制剂、免疫检查点PD-1/PD-L1、CTLA-4等药物的联用。联合疗法有可能通过显示协同或相加的抗肿瘤作用来最大限度地提高疗效,同时通过施用较低的药物剂量来降低毒性和耐药性。已上市的5个HDAC抑制剂目前都有进行多种不同药物针对不同适应症的临床试验。亿腾景昂和徐诺药业通过授权得到的两个药物也都是应用联合用药进行了实体瘤适应症的拓展且已进入临床后期。
展望
作为表观遗传学过程中重要的靶标之一,HDAC对于癌症等疾病的治疗不可或缺。随着对HDAC机理逐渐深入的研究,在探寻其与肿瘤发生和免疫千丝万缕的联系的同时,我们对疾病本身的机制和靶点途径也有了更深刻的认识。随着5个HDAC抑制剂的上市,以及多个泛HDACi和选择性HDACi进入临床试验,HDAC显然已成为新型抗癌药物的重要靶标。虽然目前HDAC抑制剂只能用于有限的血液瘤,但随着西达本胺联合用药治疗乳腺癌的获批及后续新药的申请上市, 可以预见HDAC抑制剂的适应症将得到拓展,未来将有更广的应用。相信随着科学家们的不断努力,会有越来越多高效、低毒的HDAC抑制剂应用于癌症及其它疾病的治疗。
参考文献
2020 San Antonio Breast Cancer VirtualSymposium; December 8-11, 2020; San Antonio, Texas
McClure, J.J., Li, X. and Chou, C.J (2018).Advances and challenges of HDAC inhibitors in cancer therapeutics.Advancesin cancer research,138, pp.183-211.
New, M., Olzscha, H. and La Thangue, N.B(2012).HDAC inhibitor-based therapies: can we interpret the code?Molecularoncology,6(6), pp.637-656.
Shah, R.R (2019) Safety and tolerabilityof histone deacetylase (HDAC) inhibitors in oncology.Drug safety,42(2),pp.235-245.
Shirakawa, K., Chavez, L., Hakre, S.,Calvanese, V. and Verdin, E (2013). Reactivation of latent HIV by histonedeacetylase inhibitors.Trends in microbiology,21(6),pp.277-285.
Terence C. S. Ho, Alex H. Y. Chan, and A.Ganesan (2020). Thirty Years of HDAC Inhibitors: 2020 Insight and Hindsight. Journal of Medicinal Chemistr,63(21),12460-12484.
Yeruva, S.L.H., Zhao, F., Miller,K.D.et al.(2018). E2112: randomized phase iii trial ofendocrine therapy plus entinostat/placebo in patients with hormonereceptor-positive advanced breast cancer.npj Breast Cancer, 4,1.
观研天下. 2021. 我国HDAC抑制剂行业现状:获批上市药品稀少在研药物均为口服型.http://market.chinabaogao.com/yiyao/051U433C2021.html.
生物制药小编. 2016. 表观遗传与肿瘤治疗:HDAC抑制剂类药物研究报告. https://mp.weixin.qq.com/s/rkS2BeAqFzpEr1LbfUxeJA.
药智网.2017. 揭秘抗癌先锋HDAC抑制剂. https://news.yaozh.com/archive/20989.html.
中国医药创新促进会抗肿瘤药物临床研究专业委员会(2021). 2020年度中国抗肿瘤新药临床研究评述.
